現代バイオ、前立腺がん治療の臨床試験承認

現代バイオサイエンスは、同社の環境正常化剤「フェニトリウム」を用いた前立腺がんの併用療法の臨床試験計画が、韓国食品医薬品安全処から最終承認を受けたと発表した。
同社は、21日にソウル大学病院の医学研究倫理審査委員会に関連書類を提出し、5月中旬に臨床開始会議を経て患者募集と投薬を開始する予定であると説明した。
この併用療法は、薬効減少の原因をがん細胞の変異だけでなく、腫瘍微小環境の物理的防壁による「偽耐性」にも求めている。
新たに承認された臨床変更案の核心は、患者スクリーニング段階に「AR-V7遺伝子変異検査」を追加した点である。
この検査により、受容体自体が変形して薬が効かない「真の耐性(AR-V7陽性)」患者は臨床から除外される。一方、遺伝子変異がないにもかかわらず薬が効かない「偽耐性(AR-V7陰性)」患者群のみを選別し、エンザルタミドとフェニトリウムを併用投与する。
この臨床試験が成功すれば、前立腺がん患者は深刻な副作用を伴う化学療法に移行することなく、既存の標的抗がん剤の治療効果を享受し続けることができる。
GC緑十字、血糖測定器「GGP-100」欧州CE-IVDR認証取得
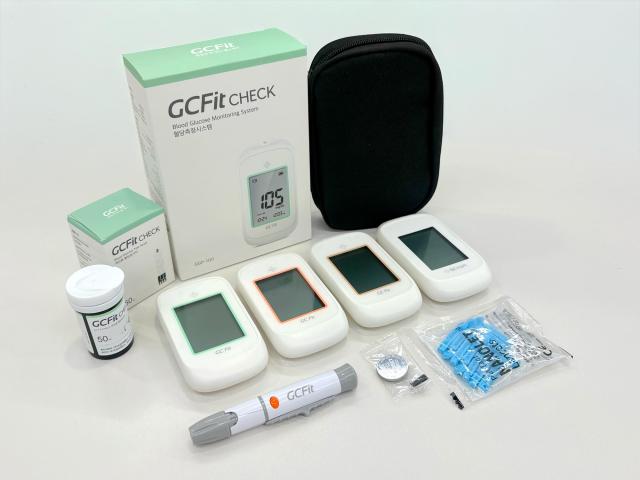
GC緑十字は、血糖事業部の新製品「GC Fit血糖測定システム(モデル名GGP-100)」が欧州連合体外診断医療機器規則(CE-IVDR)適合認証を取得したと発表した。
CE-IVDRは、既存のCE-IVDD指針に比べて性能と安全性基準が強化されたもので、EU市場への参入に必須である。
今回認証を受けたGGP-100は、高リスク群(Class-C)製品でありながら、強化された基準を満たし、製品の安全性と性能を証明した。これにより、GC緑十字は既存製品を含む血糖測定器全製品群について、欧州市場内での性能と安全性を確保した。
同社は、今回の認証により当初の計画より約2ヶ月早く欧州市場進出が可能になったと説明した。また、光学型ヘモグロビン測定製品についてもCE-IVDR認証を取得し、輸出を拡大する計画である。
* この記事はAIによって翻訳されました。
亜洲日報の記事等を無断で複製、公衆送信 、翻案、配布することは禁じられています。
